| | | | |
| | | | Procedimento
|
| | | | Indossare i guanti.
|
| | | | |
| | | | Sangue venoso raccolto in K2EDTA.
Mescolare per inversione la provetta del campione per ≈15”.
|
| | | | |
| | | | Prendere un capillare.
|
| | | | |
| | | | Riempirlo per capillarità circa fino al trattino indicatore.
|
| | | | |
| | 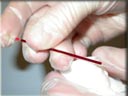
| | Far retrocedere il sangue di alcuni mm e con il dito indice tappare l’estremità opposta del capillare.
|
| | | | |
| | | | Disinfettare il capillare esternamente. |
| | | | |
| |  | | Continuando a tenere tappata l’estremità del capillare appoggiare l’estremità libera sulla plastilina.
|
| | | | |
| | 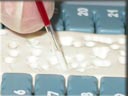 | | Affondare il capillare nella plastilina un paio di volte togliendo contemporaneamente il dito che teneva tappata l’altra estremità.
|
| | | | |
| |  | | Ripetere la stessa procedura con altri capillari posizionandoli nell’apposito supporto.
|
| | | | |
| |  | | Centrifugare i capillari a 12.000 giri per 5 minuti.
|
| | | | |
| |  | | A un vetrino portaoggetti tagliato applicare alle due estremità per tutta la sua larghezza del nastro biadesivo.
|
| | | | |
| |  | | Posizionare i capillari uno accanto all’altro sul vetrino in modo che le loro estremità poggino sul nastro biadesivo così rimarranno allo stesso.
|
| | | | |
| |  | | Poggiare un vetrino coprioggetto 24x32 sui capillari in modo da coprire la zona buffy coat.
|
| | | | |
| | 
| | Con una siringa ipodermica aggiungere molto delicatamente soluzione fisiologica nello spazio intercapillare tra vetrino portaoggetto e coprioggetto fino a che lo spazio in prossimità del buffy coat sia immerso nel liquido.
|